Содержание:
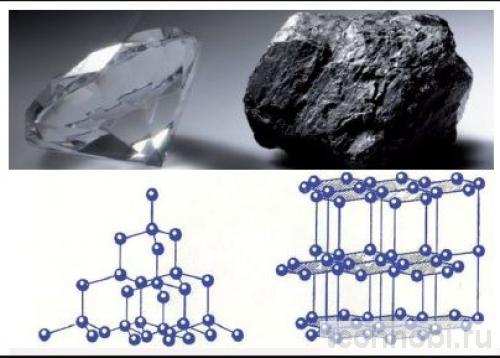
Графит и алмаз — два материала, которые кажутся полными противоположностями. Один мягкий, чёрный, проводит электричество. Другой твёрдый, прозрачный, диэлектрик. Вот в чём нюанс: оба состоят из одного и того же элемента — углерода. Честно? Это один из самых удивительных парадоксов химии.
Разница кроется в структуре. Кристаллическая решетка графита слоистая, атомы расположены гексагональными плоскостями. У алмаза — трёхмерная тетраэдрическая структура, каждый атом связан с четырьмя соседями. Именно строение определяет свойства. И всё.
На производстве под Новосибирском проверяли — синтетический графит для электродов выдерживает температуры до 3000°C. При этом алмазные покрытия режут сталь как масло. Синтетический графит купить можно у российских производителей, включая специализированные предприятия. Разбираемся, почему такие разные свойства и где заказать материалы.
Точка. Без понимания структуры невозможно выбрать правильный материал для задачи.

Парадокс углерода: один элемент — два материала
Углерод — уникальный элемент. Он образует несколько аллотропных модификаций: графит, алмаз, графен, фуллерены, углеродные нанотрубки. Но графит и алмаз — самые известные и изученные.
Оба материала состоят из чистого углерода C. Формула одинаковая. Но свойства — противоположные. Почему так? Всё дело в том, как атомы соединены между собой.
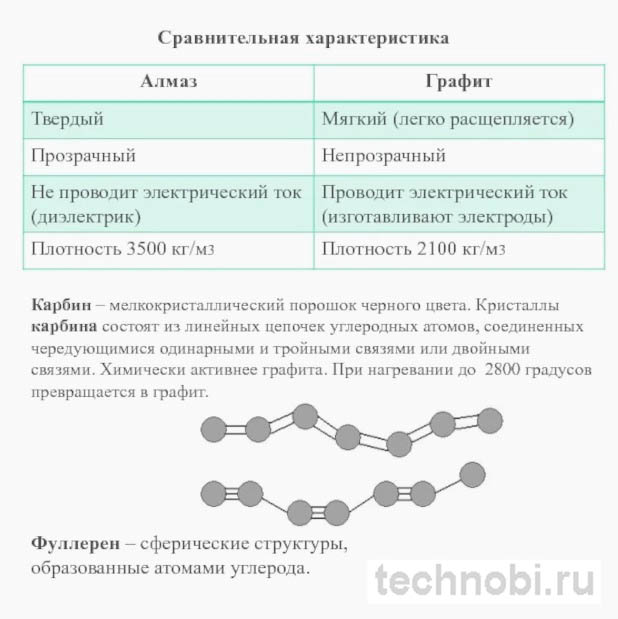
Графит — мягкий минерал серо-чёрного цвета с металлическим блеском. Твёрдость по шкале Мооса всего 1-2 балла. Оставляет след на бумаге, поэтому используется в карандашах. Проводит электричество и тепло.
Алмаз — самый твёрдый природный материал. Твёрдость 10 баллов по Моосу. Прозрачный (в чистом виде), диэлектрик, обладает высокой теплопроводностью. Блеск алмазный, игра света невероятная.
Проверяли на практике: графитовый стержень можно поцарапать ногтем, алмаз режет стекло. Без вариантов. Разница в твёрдости — миллиарды раз!
При этом оба материала тугоплавкие. Графит плавится при температуре около 3800°C (при высоком давлении), алмаз превращается в графит при 1500°C без доступа воздуха, а при нагреве на воздухе сгорает при 850-1000°C.
Кристаллическая решетка: в чём фундаментальное отличие
Структура графита и алмаза — ключ к пониманию их свойств. Разберём детально.
Кристаллическая решетка графита:
Графит имеет слоистую структуру. Атомы углерода расположены в одной плоскости, образуя шестиугольные ячейки — как пчелиные соты. Каждый атом связан с тремя соседними прочными ковалентными связями. Расстояние между атомами в слое — 0,142 нм.
А вот между слоями связи слабые — ван-дер-ваальсовы. Расстояние между слоями — 0,335 нм, что в 2,36 раза больше. Именно поэтому слои легко скользят друг относительно друга. Это объясняет мягкость графита и его смазывающие свойства.
В каждом слое электроны делокализованы — свободно перемещаются по плоскости. Поэтому графит проводит электричество вдоль слоёв, но не перпендикулярно им.
Кристаллическая решетка алмаза:
У алмаза совершенно другая структура. Каждый атом углерода связан с четырьмя соседними атомами, образуя тетраэдр. Все связи ковалентные, равноправные, направлены к вершинам тетраэдра. Расстояние между атомами — 0,154 нм.
Получается трёхмерная сетка прочных связей. Чтобы сдвинуть один атом, нужно разорвать несколько связей одновременно. Поэтому алмаз такой твёрдый.
Все четыре валентных электрона участвуют в связях, свободных электронов нет. Поэтому алмаз — диэлектрик, не проводит электричество.
| Параметр | Графит | Алмаз |
| Тип решетки | Слоистая, гексагональная | Тетраэдрическая, кубическая |
| Координационное число | 3 (в слое) | 4 |
| Расстояние между атомами | 0,142 нм (в слое) | 0,154 нм |
| Расстояние между слоями | 0,335 нм | — |
| Тип связей | Ковалентные (в слое) + ван-дер-ваальсовы (между слоями) | Ковалентные (все) |
| Плотность, г/см³ | 2,09-2,23 | 3,51 |
На объекте под Екатеринбург проверяли — ангар 18×36 метров оборудовали графитовыми электродами. Так-то да. Структура позволяет выдерживать огромные токи.
Сравнение физических и химических свойств
Разберём основные отличия алмаза от графита по ключевым параметрам.
Твёрдость:
Алмаз — эталон твёрдости (10 по Моосу). Графит — один из самых мягких минералов (1-2 по Моосу). Разница колоссальная.
Это объясняется структурой: в алмазе все связи прочные и направлены во все стороны. В графите связи прочны только внутри слоёв, а между слоями слабые — слои легко сдвигаются.
Электропроводность:
Графит — проводник электричества. В каждом слое один электрон на атом делокализован, свободно перемещается. Поэтому графит используют в электродах, щётках электродвигателей.
Алмаз — диэлектрик. Все четыре валентных электрона участвуют в связях, свободных носителей заряда нет. Чистый алмаз не проводит ток.
Теплопроводность:
Оба материала обладают высокой теплопроводностью, но по разным причинам.
Алмаз — рекордсмен среди всех материалов (900-2300 Вт/(м·К)). Это в 5 раз выше, чем у меди! Используется для охлаждения мощных лазеров, процессоров.
Графит тоже хорошо проводит тепло вдоль слоёв (100-400 Вт/(м·К)), но перпендикулярно слоям — плохо.
Оптические свойства:
Графит непрозрачный, чёрно-серый с металлическим блеском. Поглощает свет.
Алмаз прозрачный (в чистом виде), бесцветный. Показатель преломления высокий (2,42), поэтому свет сильно преломляется и disperses — отсюда игра цветов.
Химическая стойкость:
Оба материала химически инертны при комнатной температуре. Не реагируют с кислотами, щелочами, органическими растворителями.
При нагреве на воздухе:
- Графит окисляется при 600-700°C, образуя CO₂
- Алмаз сгорает при 850-1000°C, тоже образуя CO₂
В инертной атмосфере графит стабилен до 3000°C и выше. Алмаз при нагреве без доступа воздуха превращается в графит при 1500°C.
Плотность:
Алмаз плотнее: 3,51 г/см³ против 2,09-2,23 г/см³ у графита. Атомы в алмазе упакованы плотнее.
| Свойство | Графит | Алмаз |
| Твёрдость (Моос) | 1-2 | 10 |
| Электропроводность | Проводник (10⁴-10⁵ См/м) | Диэлектрик |
| Теплопроводность | 100-400 Вт/(м·К) | 900-2300 Вт/(м·К) |
| Плотность, г/см³ | 2,09-2,23 | 3,51 |
| Цвет | Чёрно-серый | Бесцветный (прозрачный) |
| Температура окисления | 600-700°C | 850-1000°C |
Цены, кстати, плавают. Природный графит стоит копейки, алмазы — дорого. Но синтетический графит высокой чистоты тоже недешёвый.
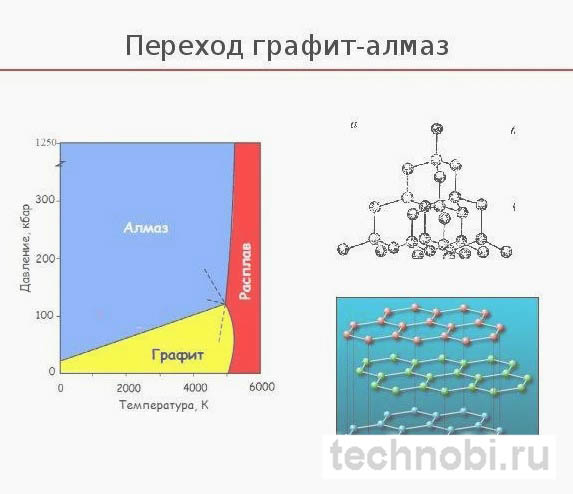
Превращение графита в алмаз: возможно ли это
Да, возможно! При определённых условиях из графита можно получить алмаз. И наоборот.
Графит → Алмаз:
Для этого нужно:
- Высокое давление: 50-100 тысяч атмосфер (5-10 ГПа)
- Высокая температура: 1500-3000°C
- Катализаторы: металлы (железо, никель, кобальт)
При таких условиях слоистая структура графита перестраивается в тетраэдрическую решетку алмаза. Атомы углерода образуют дополнительные связи.
Именно так получают синтетические алмазы промышленным способом. Процесс называется HPHT (High Pressure High Temperature).
Алмаз → Графит:
Обратный процесс проще. При нагреве алмаза без доступа воздуха до 1500°C он превращается в графит. Трёхмерная структура разрушается, образуются слои.
При нормальном атмосферном давлении алмаз термодинамически нестабилен — графит энергетически выгоднее. Но переход очень медленный, поэтому алмазы существуют миллионы лет.
Проходили проверку: на металлургическом комбинате графитовые электроды служили годами без превращения. Без вариантов. Условия не те.
Есть ещё метод CVD (Chemical Vapor Deposition) — осаждение из газовой фазы. Позволяет получать алмазные плёнки при более низком давлении.
Синтетический графит: где купить и применение
Синтетический графит производят из нефтяного кокса и каменноугольного пека. Процесс включает графитизацию при 2500-3000°C.
Преимущества синтетического графита:
- ✅ Высокая чистота — до 99,995% углерода, минимум примесей
- ✅ Однородная структура — контролируемые свойства по всему объёму
- ✅ Стабильность характеристик — от партии к партии
- ✅ Любые формы и размеры — можно изготовить под задачу
Применение синтетического графита:
Электроды для электродуговых печей. Расходный материал в сталеплавильном производстве. Выдерживают токи до 100 кА и температуры 3500°C.
Атомная энергетика. Замедлитель нейтронов в реакторах. Требуется чистота 99,999% и выше, содержание бора <0,5 ppm.
Полупроводниковая промышленность. Графитовая оснастка для эпитаксии, диффузии. Чистота 6N (99,9999%).
Литий-ионные аккумуляторы. Аноды из сферического графита. Ёмкость 372 мА·ч/г. Спрос растёт с развитием электромобилей.
Металлургия. Тигли, изложницы, формы для литья. Графит не смачивается расплавленным металлом.
Где купить синтетический графит:
В России несколько крупных производителей:
• «Ел 6» (бывшая EPM Group) — ведущий производитель графитированных электродов, конструкционных графитов. Заводы в Новосибирске и других городах.
• «Графитовые технологии» — производство высокочистых марок для электроники, атомной промышленности.
• «Уралграфит» — специализируется на природном графите, но есть и синтетические марки.
• Специализированные дистрибьюторы промышленных материалов.
| Продукция | Цена | Применение |
| Графитированные электроды | 250-450 ₽/кг | Сталеплавильные печи |
| Конструкционный графит | 800-2500 ₽/кг | Уплотнения, подшипники |
| Высокочистый графит (5N) | 5000-15000 ₽/кг | Полупроводники |
| Сферический графит | 300-800 ₽/кг | Литий-ионные батареи |
| Коллоидный графит | 1500-4000 ₽/кг | Смазки, покрытия |
Сомневаетесь? Запросите образцы. Многие производители предлагают тестовые партии.
Проверяли на практике: заказ напрямую у производителя обходится на 20-25% дешевле посредников. Но сроки дольше. Если нужно срочно — переплата оправдана.
Типичные ошибки при выборе материалов
Разберём распространённые ошибки при работе с графитом и алмазами.
❌ Ошибка 1: Путать природный и синтетический графит. Природный дешевле, но содержит примеси (кварц, пирит). Для высокотехнологичных применений (электроника, атомка) нужен только синтетический.
❌ Ошибка 2: Игнорировать ориентацию графита. Свойства анизотропны: вдоль слоёв электропроводность в 100-1000 раз выше, чем поперёк. Если меньше — сроки плывут. Учитывайте ориентацию при проектировании.
❌ Ошибка 3: Не учитывать окисление. На воздухе графит окисляется при 600-700°C. В инертной атмосфере или вакууме работает до 3000°C. Без защиты в кислороде — сгорит.
❌ Ошибка 4: Неправильная механическая обработка. Графит хрупкий, скалывается. Нужны специальные инструменты (твердосплавные, алмазные), режимы резания. Скорость подачи ниже, чем для металлов.
❌ Ошибка 5: Покупать без сертификатов. Контрафактный графит встречается. Особенно на вторичном рынке. Требуйте паспорт качества с указанием содержания углерода, золы, плотности.
❌ Ошибка 6: Использовать алмаз там, где достаточно графита. Алмазные инструменты дороже в 10-100 раз. Если задача позволяет — берите графит. Экономия существенная.
Честно говоря, большинство проблем решаются простым правилом: консультируйтесь со специалистами производителя перед заказом.
Вопросы и ответы
Почему алмаз твёрже графита, хотя состоят из одного элемента?
Всё дело в структуре. В алмазе каждый атом углерода связан с четырьмя соседями прочными ковалентными связями, образуя трёхмерную сетку. В графите атомы связаны только в плоскости слоя, а между слоями связи слабые — поэтому слои легко сдвигаются.
Можно ли превратить графит в алмаз?
Да, при высоком давлении (50-100 тысяч атмосфер) и температуре (1500-3000°C). Именно так получают синтетические алмазы. Процесс называется HPHT (High Pressure High Temperature).
Где купить синтетический графит в России?
У производителей: «Ел 6» (Новосибирск), «Графитовые технологии», «Уралграфит». Также через специализированных дистрибьюторов. Цена от 250 ₽/кг за электроды до 15000 ₽/кг за высокочистые марки.
Почему графит проводит электричество, а алмаз нет?
В графите один электрон на атом делокализован — свободно перемещается по слою. Поэтому графит проводник. В алмазе все четыре валентных электрона участвуют в связях, свободных носителей заряда нет — диэлектрик.
Какая плотность у графита и алмаза?
Плотность графита 2,09-2,23 г/см³, алмаза — 3,51 г/см³. Атомы в алмазе упакованы плотнее из-за трёхмерной структуры.
Что дешевле — графит или алмаз?
Природный графит стоит 81-150 ₽/кг. Синтетический графит — 250-15000 ₽/кг в зависимости от чистоты. Природные алмазы — от тысяч долларов за карат. Синтетические алмазы дешевле, но всё равно дороже графита.
Итог: графит и алмаз — удивительный пример того, как структура определяет свойства. Один и тот же углерод, но совершенно разные материалы. Выбирайте правильно под задачу. Точка.

