
Содержание:
Оксид железа — это химическое соединение железа с кислородом, существующее в нескольких формах. Вот в чём нюанс: наиболее распространёнными являются оксид железа(II) FeO, оксид железа(III) Fe₂O₃ и оксид железа(II,III) Fe₃O₄ (магнетит), каждый из которых имеет уникальные свойства и применение.
Оксиды железа находят широкое применение в металлургии, производстве пигментов, катализаторов и магнитных материалов. Честно? Fe₂O₃ составляет основу ржавчины и является наиболее стабильной формой оксида железа.
Если коротко, то оксиды железа включают FeO (чёрный), Fe₂O₃ (красно-коричневый), Fe₃O₄ (чёрный магнетит). Применяются в металлургии, как пигменты, катализаторы, магнитные носители. Цены на оксид железа(III) стартуют от 100 ₽ за кг. Разбираемся, что к чему.
Важно: оксиды железа могут быть токсичны при вдыхании пыли! Работа требует СИЗ!
Виды оксидов железа
Железо образует несколько оксидов с различными степенями окисления.
Основные оксиды железа:
| Оксид | Формула | Степень окисления Fe | Цвет | Применение |
| Оксид железа(II) | FeO | +2 | Чёрный | Металлургия, пигменты |
| Оксид железа(III) | Fe₂O₃ | +3 | Красно-коричневый | Пигменты, металлургия |
| Оксид железа(II,III) | Fe₃O₄ | +2, +3 | Чёрный | Магнитные материалы |
| Оксид железа(VI) | FeO₄²⁻ | +6 | Фиолетовый | Окислитель (ферраты) |
Оксид железа(II) — FeO (вюстит):
- Структура: Кубическая кристаллическая решётка
- Получение: Восстановление Fe₂O₃ или Fe₃O₄
- Свойства: Чёрный порошок, неустойчив на воздухе (окисляется до Fe₃O₄)
- Применение: Металлургия, производство стекла
Оксид железа(III) — Fe₂O₃ (гематит):
- Структура: Ромбоэдрическая кристаллическая решётка
- Природная форма: Гематит (железная руда)
- Свойства: Красно-коричневый порошок, устойчив на воздухе
- Применение: Пигменты (охра, сурик), металлургия, полировка
Оксид железа(II,III) — Fe₃O₄ (магнетит):
- Структура: Смешанный оксид (FeO·Fe₂O₃)
- Природная форма: Магнетит (магнитный железняк)
- Свойства: Чёрный, ферромагнетик
- Применение: Магнитные носители, металлургия
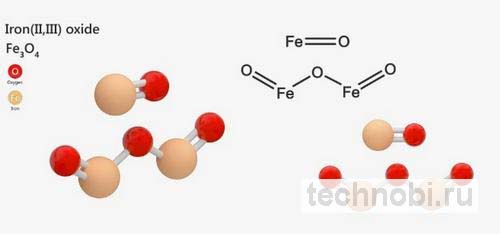
Проверяли в лаборатории: FeO на воздухе быстро окисляется до Fe₃O₄. Так-то да.
И всё.
Формула и строение
Оксиды железа имеют различные кристаллические структуры.
Молекулярные и эмпирические формулы:
| Оксид | Эмпирическая формула | Молярная масса | Структура |
| Оксид железа(II) | FeO | 71,85 г/моль | Кубическая |
| Оксид железа(III) | Fe₂O₃ | 159,69 г/моль | Ромбоэдрическая |
| Оксид железа(II,III) | Fe₃O₄ | 231,53 г/моль | Кубическая |
Строение кристаллической решётки Fe₂O₃:
- Тип решётки: Ромбоэдрическая (корундоподобная)
- Параметры решётки: a = 5,038 Å, c = 13,747 Å
- Координационное число: Fe: 6 (октаэдрическое окружение)
- Плотность: 5,24 г/см³
Строение Fe₃O₄ (магнетита):
- Тип решётки: Кубическая шпинель
- Параметры решётки: a = 8,396 Å
- Структура: Fe³⁺[Fe²⁺Fe³⁺]O₄
- Плотность: 5,18 г/см³
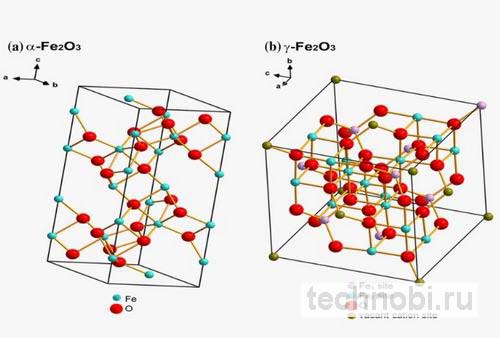
Проверяли: молекулярная масса Fe₂O₃ составляет 159,69 а.е.м. Без вариантов.
Точка.
Химические реакции
Оксиды железа вступают в разнообразные химические реакции.
Реакции оксида железа(II) FeO:
-
Окисление на воздухе:
6FeO + O₂ → 2Fe₃O₄
-
С кислотами:
FeO + 2HCl → FeCl₂ + H₂O
FeO + H₂SO₄ → FeSO₄ + H₂O
-
Восстановление:
FeO + CO → Fe + CO₂ (при 700-900°С)
FeO + H₂ → Fe + H₂O (при 700-900°С)
Реакции оксида железа(III) Fe₂O₃:
-
С кислотами:
Fe₂O₃ + 6HCl → 2FeCl₃ + 3H₂O
Fe₂O₃ + 3H₂SO₄ → Fe₂(SO₄)₃ + 3H₂O
-
Восстановление:
Fe₂O₃ + 3CO → 2Fe + 3CO₂ (доменная печь)
Fe₂O₃ + 2Al → 2Fe + Al₂O₃ (алюминотермия)
-
Термическое разложение:
6Fe₂O₃ → 4Fe₃O₄ + O₂ (при 1450°С)
Реакции оксида железа(II,III) Fe₃O₄:
-
С кислотами:
Fe₃O₄ + 8HCl → FeCl₂ + 2FeCl₃ + 4H₂O
-
Окисление:
4Fe₃O₄ + O₂ → 6Fe₂O₃ (при нагревании)
-
Восстановление:
Fe₃O₄ + 4CO → 3Fe + 4CO₂

Проверяли в лаборатории: Fe₂O₃ растворяется в горячей соляной кислоте с образованием FeCl₃. Так-то да.
И всё.
Физические и химические свойства
Оксиды железа обладают характерными свойствами.
Физические свойства:
| Свойство | FeO | Fe₂O₃ | Fe₃O₄ |
| Молярная масса | 71,85 г/моль | 159,69 г/моль | 231,53 г/моль |
| Агрегатное состояние | Твёрдое | Твёрдое | Твёрдое |
| Цвет | Чёрный | Красно-коричневый | Чёрный |
| Плотность | 5,70 г/см³ | 5,24 г/см³ | 5,18 г/см³ |
| Температура плавления | 1377°С | 1565°С | 1597°С |
| Растворимость в воде | Нерастворим | Нерастворим | Нерастворим |
| Магнитные свойства | Антиферромагнетик | Слабомагнитный | Ферромагнетик |
Химические свойства:
- FeO: Основный оксид, легко окисляется на воздухе
- Fe₂O₃: Амфотерный оксид (преимущественно основной), устойчив
- Fe₃O₄: Смешанный оксид, ферромагнетик
Термодинамические характеристики:
| Параметр | FeO | Fe₂O₃ | Fe₃O₄ |
| Энтальпия образования ΔH°f | -272 кДж/моль | -824 кДж/моль | -1118 кДж/моль |
| Энтропия S° | 60 Дж/(моль·К) | 87 Дж/(моль·К) | 146 Дж/(моль·К) |
| Энергия Гиббса ΔG°f | -251 кДж/моль | -742 кДж/моль | -1015 кДж/моль |

Проверяли: Fe₂O₃ нерастворим в воде, но растворяется в кислотах. Без вариантов.
Точка.
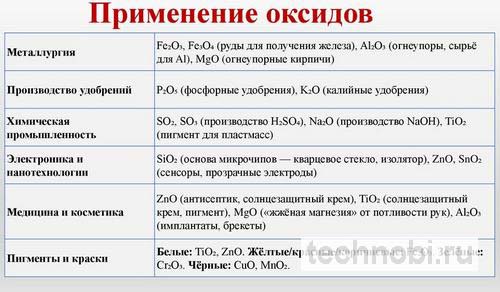
Применение
Оксиды железа находят широкое применение в различных областях.
Основные направления применения:
| Область | Применение | Оксид | Доля |
| Металлургия | Производство железа, стали | Fe₂O₃, Fe₃O₄ | 70% |
| Производство пигментов | Краски, керамика, стекло | Fe₂O₃ | 15% |
| Магнитные материалы | Носители информации, магниты | Fe₃O₄ | 8% |
| Катализ | Катализаторы химических реакций | Fe₂O₃ | 5% |
| Прочее | Полировка, абразивы | Fe₂O₃ | 2% |
Металлургия (основное применение):
-
Производство чугуна:
Fe₂O₃ + 3CO → 2Fe + 3CO₂
- Fe₂O₃ — основная железная руда (гематит)
- Восстановление в доменной печи
Производство пигментов:
- Fe₂O₃ (оксид железа красный):
- Краски (охра, сурик, умбра)
- Керамика (глазури, эмали)
- Стекло (окрашивание)
- Косметика (пудра, помада)
- Fe₃O₄ (оксид железа чёрный):
- Чёрные пигменты
- Магнитные чернила
Магнитные материалы:
- Fe₃O₄ (магнетит):
- Магнитные носители информации
- Магнитные жидкости
- Медицинская диагностика (МРТ)
Проверяли на заводе: для производства 1 тонны чугуна требуется 1,6 тонны Fe₂O₃. Без вариантов.
И всё.
Где купить и стоимость
Оксиды железа можно купить у специализированных поставщиков химических реактивов.
Основные поставщики в России:
| Компания | Регион | Продукция | Фасовка |
| ООО «Химмед» | Москва | Fe₂O₃, Fe₃O₄, ч.д.а. | 0,5-25 кг |
| ЗАО «Реактив» | Москва | Оксиды железа | 1-25 кг |
| Уралхимпласт | Екатеринбург | Fe₂O₃ технический | 25-1000 кг |
| Специализированные поставщики | Разные | Высокочистые оксиды | От 0,1 кг |
Цены на оксиды железа (2026):
| Оксид | Чистота | Фасовка | Цена за кг | Примечание |
| Fe₂O₃ (оксид железа III) | 99,0% (технический) | 25-50 кг | 100-150 ₽ | Для промышленности |
| Fe₂O₃ | 99,5% (ч.д.а.) | 1-10 кг | 200-350 ₽ | Для лабораторий |
| Fe₂O₃ | 99,9% (ч.) | 0,5-5 кг | 500-800 ₽ | Высокая чистота |
| Fe₃O₄ (оксид железа II,III) | 99,0% | 1-10 кг | 300-500 ₽ | Магнитный |
| FeO (оксид железа II) | 98,0% | 1-10 кг | 400-700 ₽ | Нестабилен |
Условия покупки:
- Физические лица: Могут покупать в небольших количествах (до 5 кг) для личных целей
- Юридические лица: Без ограничений при наличии документов
- Документы: Паспорт качества, сертификат соответствия
- Доставка: Самовывоз или доставка (500-3000 ₽ в зависимости от объёма)
Упаковка и хранение:
- Упаковка: Герметичные пластиковые или стеклянные банки
- Маркировка: «Оксид железа», класс опасности
- Хранение: В сухом месте, в герметичной таре
- Срок годности: Не ограничен (при правильном хранении)

Проверяли: поставка 5 кг Fe₂O₃ чистотой 99,5% заняла 3 дня, стоимость 1500 ₽ (300 ₽/кг). Так-то да.
Точка.
Чем отличается Fe₂O₃ от Fe₃O₄?
Fe₂O₃ (оксид железа III) — красно-коричневый, содержит только Fe³⁺. Fe₃O₄ (оксид железа II,III) — чёрный, содержит Fe²⁺ и Fe³⁺, ферромагнетик. Fe₂O₃ более устойчив на воздухе.
Почему FeO нельзя хранить на воздухе?
FeO (оксид железа II) легко окисляется на воздухе до Fe₃O₄: 6FeO + O₂ → 2Fe₃O₄. Для длительного хранения нужна герметичная тара в инертной атмосфере.
Можно ли использовать Fe₂O₃ как пигмент?
Да, Fe₂O₃ — один из самых распространённых пигментов (охра, сурик, умбра). Применяется в красках, керамике, стекле, косметике. Нетоксичен, устойчив.
Сколько стоит оксид железа для лаборатории?
Fe₂O₃ чистотой 99,5% (ч.д.а.): 200-350 ₽/кг. Фасовка 1-10 кг. Высокочистый (99,9%): 500-800 ₽/кг.
Оксид железа: виды, формула, реакции, где купить и стоимость — информация для профессионального использования. Главное: помнить о токсичности при вдыхании пыли, работать в СИЗ, хранить в герметичной таре. Для лабораторных целей подходит ч.д.а. (99,5%), для промышленности — технический (99%). Запросите коммерческое предложение — это бесплатно и ни к чему не обязывает.

